原発性線毛運動不全症。
複雑で長い病名です。
線毛機能不全症候群
( primary ciliary dyskinesia, PCD )
とも呼ばれます。
原発性とは、”原因が特定できない”という意味です。病名からは、何か”線毛運動”に異常がある病気らしい…と推測できます。
今回は、全身的な疾患であるけれど耳鼻咽喉科の外来にもやってくる、この稀な疾患について書きます。
原発性線毛運動不全症とは?
原発性線毛運動不全症( primary ciliary dyskinesia, PCD) とは、気道粘膜上皮に存在する線毛(cilia)の機能に異常がある疾患です。
線毛機能不全症候群とも呼ばれています。
遺伝性疾患で多くは常染色体劣性遺伝により発症します。発症頻度は約2万人に1人です。
(以下の文章中の多くの図や写真を、信頼できる専門性を有するweb上のサイト、Wikipedia から引用しています。興味のある方はサイトへのリンクを貼っていますのでご参照ください。)
線毛とは?
この疾患を理解するには、線毛について知らなければなりません。
線毛とは、副鼻腔や気管支などの粘膜の表面にある非常に細い”毛の集まり”です。

走査電子顕微鏡(SEM)画像
https://en.m.wikipedia.org/wiki/Cilium
副鼻腔や気管支などの粘膜上には、粘液層(mucus layer)と呼ばれる粘液のバリアが存在し、粘膜を保護するとともに、粘液層をベルトコンベアのように移動させて、体内の異物を除去する”清掃作業のような”働きをもっています。
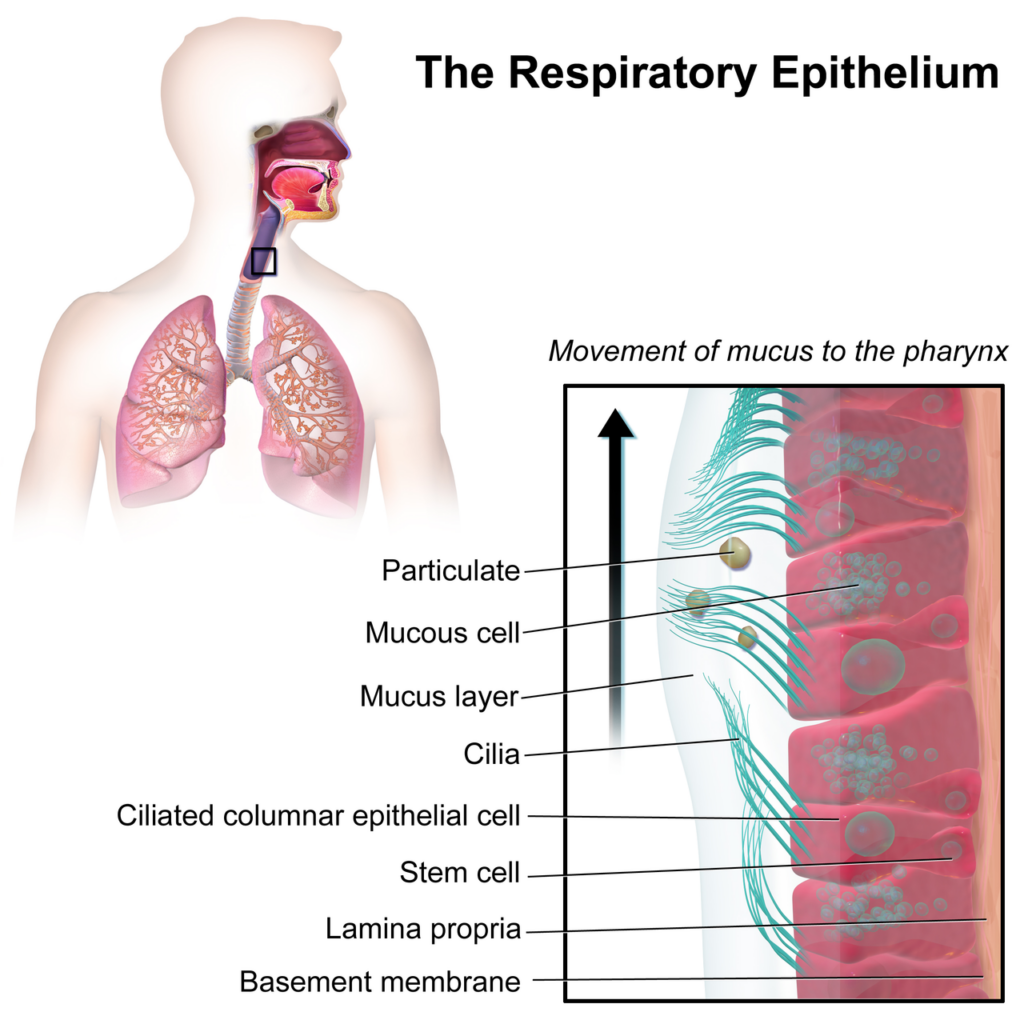
https://en.m.wikipedia.org/wiki/Mucus
線毛(cilia)の運動によって粘液層(mucus layer)を矢印(↑)の方に移動させて、異物(particulate)を体外へ排出させます。
線毛の運動は、細い”毛”を一定方向に”波打つように”動かします。大きく抵抗の強いストロークと小さく抵抗の少ないストロークを反復することで、一定方向への水流を生み出して、粘液層を1方向へ送り出しています。
大きなストロークを有効打(effctive stroke)、小さなストロークを回復打(recovery stroke)と呼んでいます。 (図1)
線毛運動は理解できました。その意味も。
では何故、線毛は動くことができるのでしょう。
そのためには線毛の微小構造を知る必要があります。
線毛の構造
線毛を輪切りにすると、このような構造をしています。
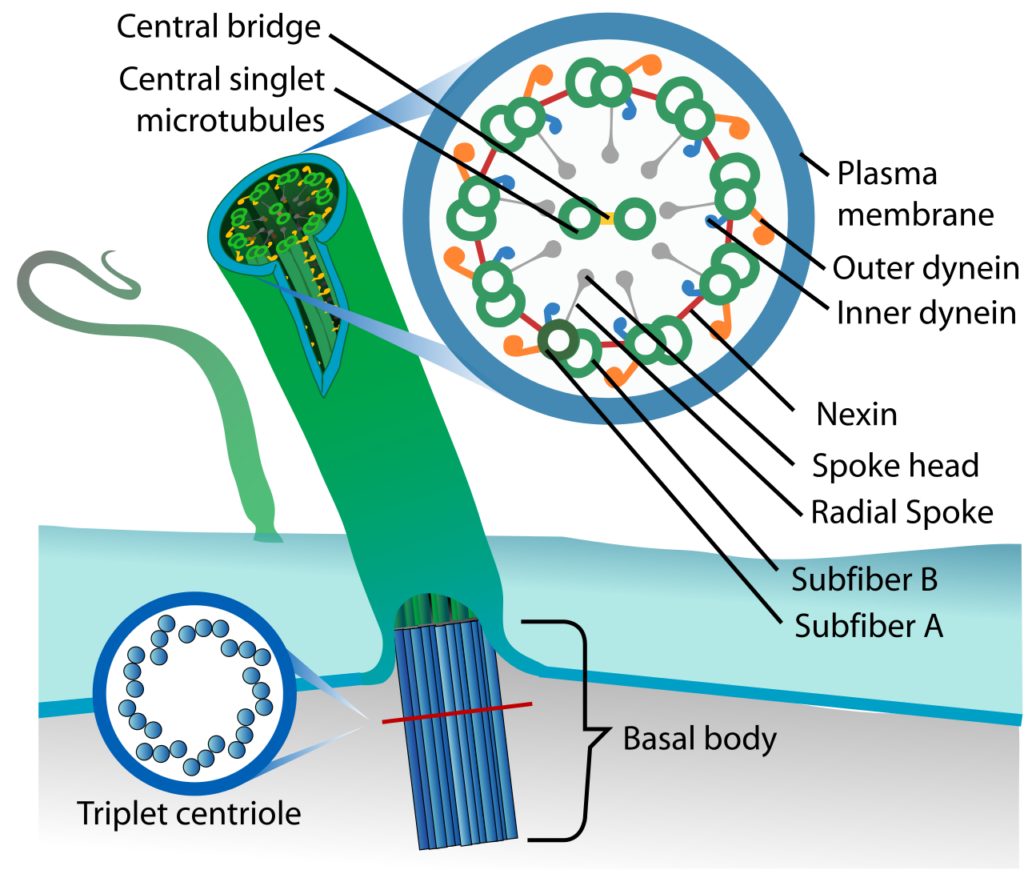
https://en.m.wikipedia.org/wiki/Cilium
上図で、緑色の太い棒状のものが1本の線毛(cilium)です。基部はbasal body の部分で上皮細胞に接着しています。
線毛(cilium)の断面が示されています。
cilium 断面の中にある、緑色🟩の小さなリング状の管腔構造物が微小管(microtubules)と呼ばれるものです。
多くの真核生物の線毛は、中心部分に2本の微小管(microtubules)が1対になって存在し、その全周を2本1対、9対の微小管(microtubules)が取り巻いている構造をしています。(9+2 構造)
微小管(microtubules)は、nexin, radial spoke などの構造物で周囲に固定されていて、 microtubule 上には、モータータンパクの1種であるダイニン(dynein)、キネシン(kinesin)が結合しています。 (図2)
微小管
微小管(microtubule) は、α-tubulin, β-tubulin の2個のチューブリン(tubulin)が結合した2量体を基本単位として構成されます。この2量体が繊維状に繋がってプロトフィラメント (protofilament) と呼ばれる鎖を形成し、このプロトフィラメントが13本並んで螺旋状の管腔を構成します。これが微小管(microtubule)です。 (図3)
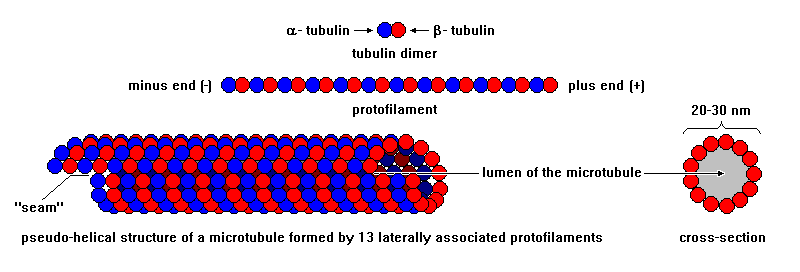
青色🟦α-tubulin, 赤色🟥β-tubulin,
protofilament, microtubule
https://ja.m.wikipedia.org/wiki/%E5%BE%AE%E5%B0%8F%E7%AE%A1
微小管は、α-tubulin とβ-tubulin の2個のタンパクが結合してダイマー(2量体)を形成し、これがたくさん重合して螺旋状の管腔構造物になったものです。(図3)
微小管(microtubules)は、伸長と短縮を繰り返しており、重合を続けていた微小管が突然、脱重合を起こして短時間に分解するような動的不安定性(dynamic instability) を有しています。
微小管が重合と脱重合を繰り返す反応は、微小管のダイナミクスと呼ばれています。
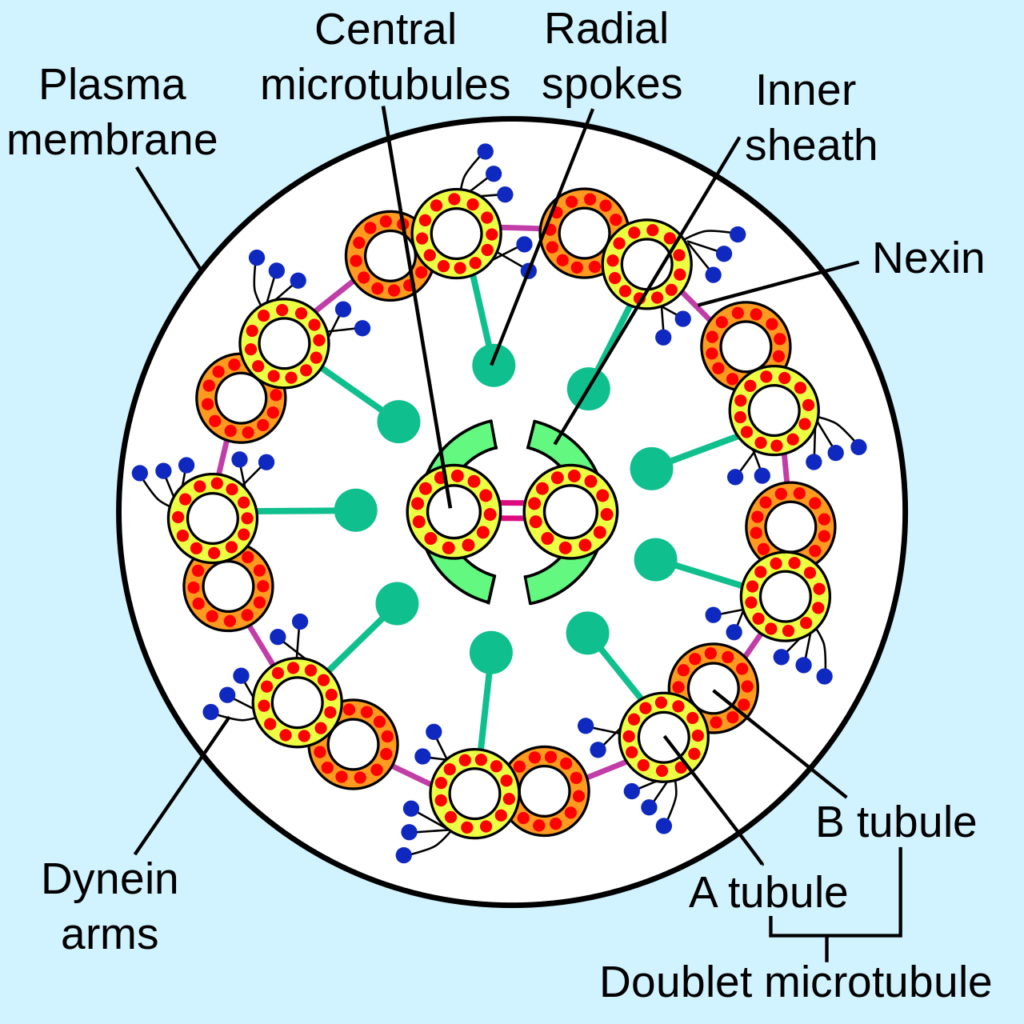
A tubule, B tubule が重合して
doublet (2本1対)のmicrotubulesを構成
https://en.m.wikipedia.org/wiki/Axoneme
運動機能を有する線毛は、運動線毛 (motile cilia )と呼ばれます。
線毛(cilium)は、軸糸(axoneme) の中心にある2本の中心微小管(singlet microtubule) と周囲の9本の周辺微小管(doublet microtubules) で構成されています。(9+2 axoneme)
線毛には一次線毛(primary cilia)もあり、これは中心の1対のmicrotubules 2本を欠き、9本のmicrotubules のみで構成されます。(9+0 axoneme)
運動しない線毛は、ダイニン(dynein)と呼ばれるmotor タンパクを欠いています。
微小管上を動くモータータンパク、
ダイニンとキネシン
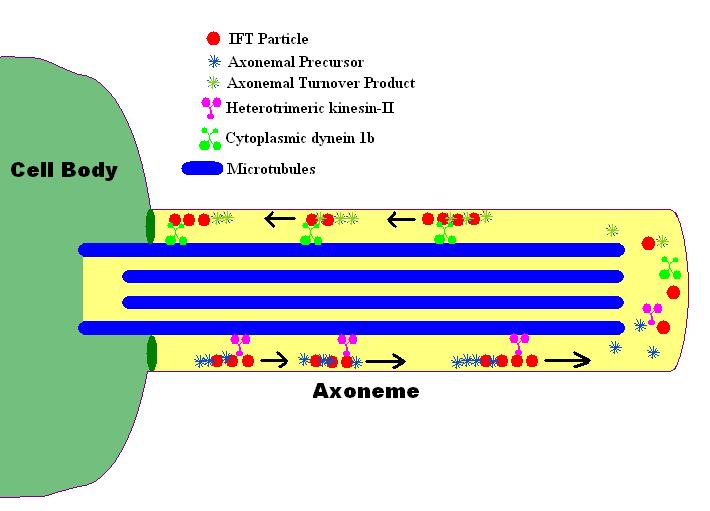
緑色🟩ダイニン(dynein)
ピンク色 キネシン(kinesin)
https://en.m.wikipedia.org/wiki/Axoneme
モータータンパクのダイニン(dynein)とキネシン(kinesin)がmicrotubule上を動きます。ダイニンはcilium先端から細胞方向へ、キネシンは細胞からcilium先端方向へと、動く方向性が決まっています。
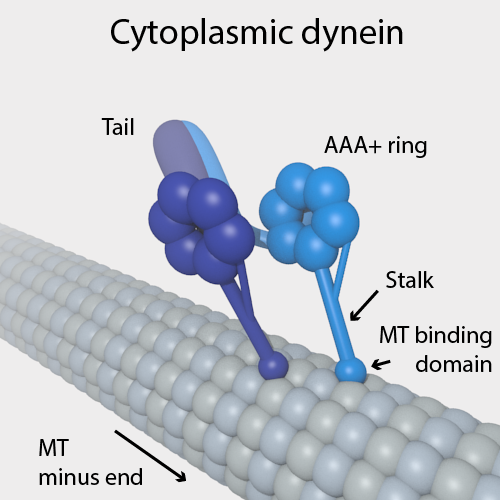
微小管(microtubule=MT)上を
マイナス方向へ移動する
https://en.m.wikipedia.org/wiki/Dynein
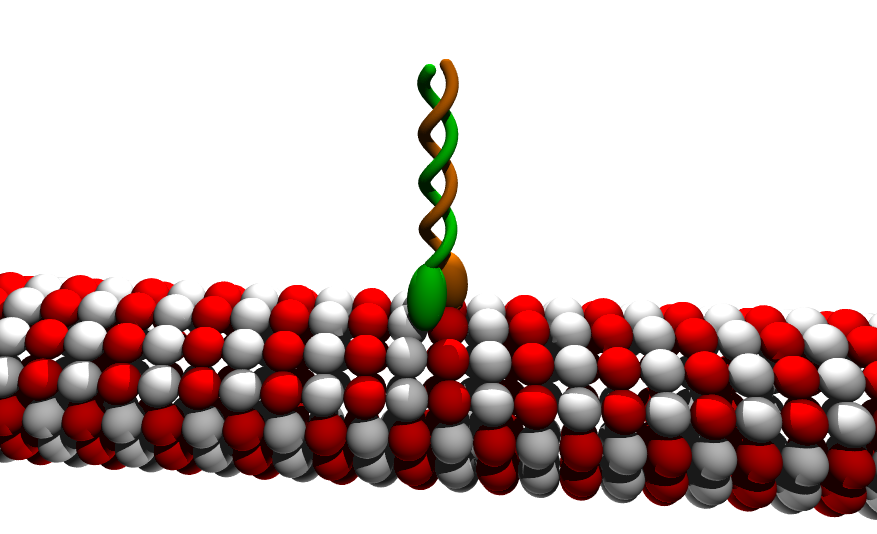
微小管(microtubule =MT)上を
プラス方向へ移動する
https://en.m.wikipedia.org/wiki/Microtubule
https://en.m.wikipedia.org/wiki/Kinesin
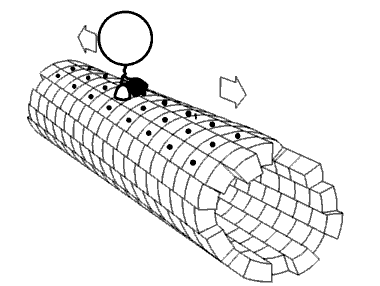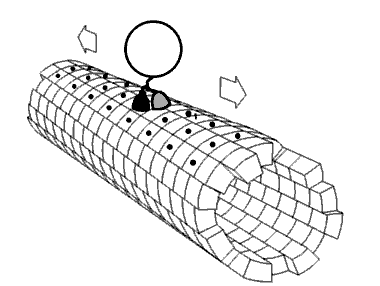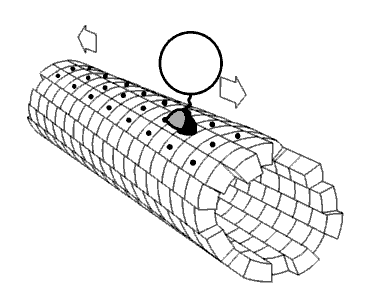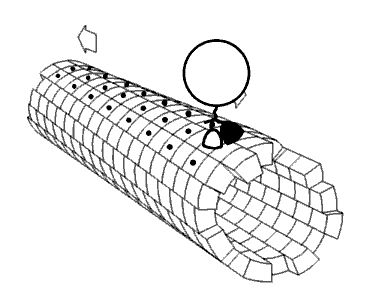
キネシンは微小管上を、ATPを加水分解してADPに変換する反応を繰り返しながら両脚を手繰り寄せるように、微小管との接着と解離を繰り返して、あたかも”歩くように”進んでいくと考えられています。
これをHand-Over-Hand Model と言います。
ダイニンとキネシンが、線毛運動に深く関係しています。とくにダイニンの腕(arm)の欠損がこの疾患、”原発性線毛運動不全症”の最も大きな原因であることが解明されてきています。
微小管 (microtubule) とは、線毛だけに存在するのではなく、じつは細胞内骨格を構成する大きな成分の一つになっています。(写真2)
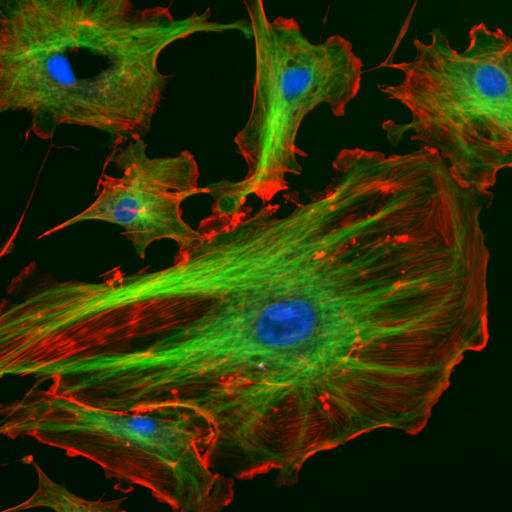
(赤色🟥 actin filament, 緑色🟩 microtubules)
アクチンフィラメント(actin filament)と
微小管(microtubules)は細胞内骨格を形成している
https://en.m.wikipedia.org/wiki/Microtubule
細胞内のタンパク質輸送に、微小管がレールの役目をしながらうまく利用されています。
細胞内の微小管上もダイニンとキネシンが移動しています。
基礎医学的な説明が長くなりましたが、
” 線毛運動は微小管に沿ってモータータンパクが動くことで起こること” を理解してください。
ダイニンの動きと微小管のねじれ
線毛運動は、線毛内に存在する微小管(microtubule) 上を移動するダイニン(dynein)と呼ばれるモータータンパクに何か異常があるとき、線毛運動に異常が出ることがわかっています。
微小管上のダイニンがATPを加水分解してエネルギーを取り出し、これが9対ある2本の微小管(A tubuleとB tubule)の滑り(すべり)運動に変換されて、線毛の屈曲が引き起こされると考えられています。 (図4)
ダイニンが微小管上をどのように動くと微小管の滑り運動が生じたり、屈曲運動が生じるのか、これに関してはいくつかの実験結果から検証されています。 (図9, 10)
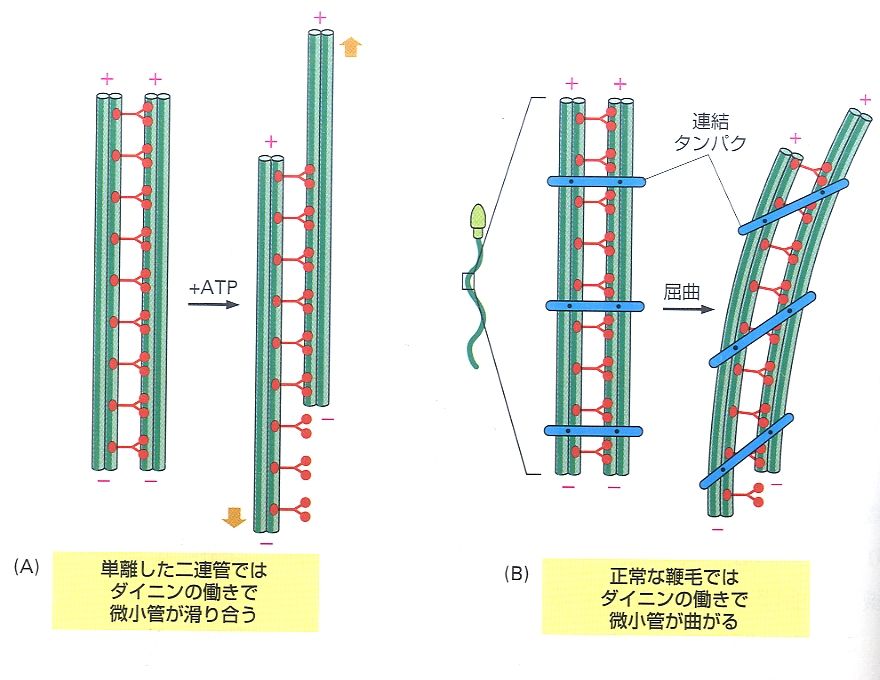
微小管の滑り運動(左)と屈曲運動(右)
https://manabu-biology.com/archives/48899634.html
(微小管による運動-鞭毛の構造と曲がる仕組み- バイオハックch より引用)
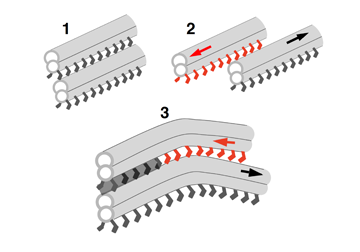
赤🟥微小管の上を動くダイニン
グレー(網掛け)微小管の上で動かないダイニン
http://shochou-kaigi.org/interview/interview_38/
(細胞はなぜ「毛」を持つのか――
生物進化のカギを握る鞭毛・繊毛に迫る
筑波大学下田臨海実験センター長 稲葉 一男 教授 2017年6月22日 より引用)
ダイニンのパワープルモデル (power pull model)
(軸糸ダイニンの構造と仕組み 吉川雅英,八木俊樹 京都大学大学院理学研究科)
https://www.jstage.jst.go.jp/article/biophys/48/6/48_6_325/_pdf
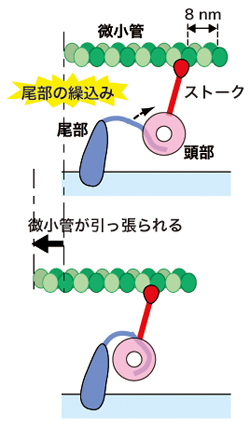
ストークを引っ張り微小管を8 nm 滑らせる
https://www.s.u-tokyo.ac.jp/ja/press/2008/26.html
(研究成果紹介「細胞内を移動するタンパク質「ダイニン」が 動いているときの構造が見えた!—細胞内の物質輸送を行う分子モーターが動く仕組みの解明へ—」
中央大学公式you tube )
興味のある方はぜひ、上記サイトをご覧ください。
ダイニンの外腕
ダイニンには外腕と内腕があります。
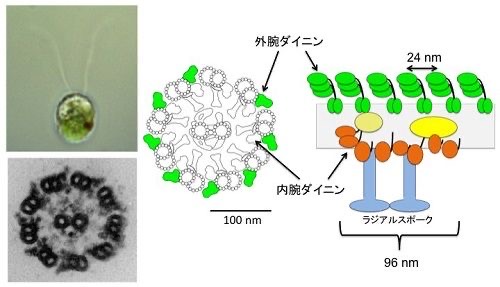
内腕ダイニン(オレンジ色🟧)
http://www.res.titech.ac.jp/news/reserch/post_25.html
外腕ダイニンは24 nm 間隔で並び、内腕ダイニンは96 nm 間隔で並んでいます。
A-tubule の外腕ダイニンが隣のペアのB-tubule に接着して、(先に書いた)ダイニンの運動で微小管と微小管の滑り運動を引き起こします。線毛運動をコントロールする微小管の動きのうち2/3が外腕ダイニンの動きによって発生していることが報告されています。
そのため、線毛運動の異常は外腕ダイニンに異常があるときに多く起こるとされています。
ダイニン外腕の異常で線毛運動に異常が起こる
基礎医学の知識の理解にかなりの紙面を費やしました。やや難解だと思いますが、じつは基礎医学は臨床医学を支える土台となる重要な学問です。
線毛運動は微小管の動きによって起こり、微小管はダイニンというモータータンパクの動きによって起こることが理解できました。
原因遺伝子
PCDの原因遺伝子は、近年次々と発見されています。現在までに50以上の遺伝子が報告されています。
遺伝子異常による発現は、①外腕ダイニンの欠損が、ARMC4, CCDC103, DNAH5など10遺伝子、②内腕ダイニンと外腕ダイニンの欠損が、CFAP298, DNAAF1, DNNAF4など11遺伝子、③内腕ダイニンの欠損と微小管構造の異常が、CCDC39, CCDC40の2遺伝子、④線毛形態が正常であるもの、CCDC65, CFAP221, DRC1など7遺伝子、⑤その他の遺伝子となっています。
欧米ではDNAH5遺伝子が多く、ダイニン外腕の欠損を起こします。
一方、国内ではダイニン内腕の欠損によるPCD診断が多いとされていますが、日本ではDRC1遺伝子が多く、ネキシン−ダイニン制御複合体の大規模欠失を起こします。DRC1遺伝子は、人口の0.2%に存在しているとされており、この遺伝子のホモ接合体(AA, BB, aa, bb )がPCD発症の原因になっていることが報告されています。
いずれにせよ、PCDは多くの場合、外腕ダイニンの欠損が原因となって微小管の運動障害を引き起こし、線毛運動機能不全を発症することが知られています。
遺伝子検査によるPCDの診断確率は、現在までに70%となっています。
原発性線毛運動不全症(PCD)
原発性線毛運動不全症 (primary ciliary dyskinesia, PCD) は、線毛運動が起こらない、または低下した疾患です。
症状として何が起こるかは、線毛がどこにあるかに深く関係してきます。
線毛は、気管、気管支、鼻腔、副鼻腔、耳管、中耳、卵管などに存在する粘膜上皮の表面を覆うように存在しています。

走査電子顕微鏡(SEM)画像
https://en.m.wikipedia.org/wiki/Cilium
先に書いた、線毛運動の機能を持ち、線毛が波打つように有効打と回復打を繰り返すことで、一定方向に水流を発生させて、線毛上の粘液層をベルトコンベアのように押し流し、異物の排出を行なっています。
線毛は気道上皮に多い
とくに気管や気管支粘膜上には、吸気時に多くの粉塵(ダスト)を吸い込むため、肺の奥まで入り込まないように、これを粘液層で補足しています。粘液層で補足した粉塵はそのままでは排泄されませんから、粘膜の線毛運動によって気管支の中枢方向へ押し戻され、最終的には”痰”となって気管から咽頭へ排出されています。
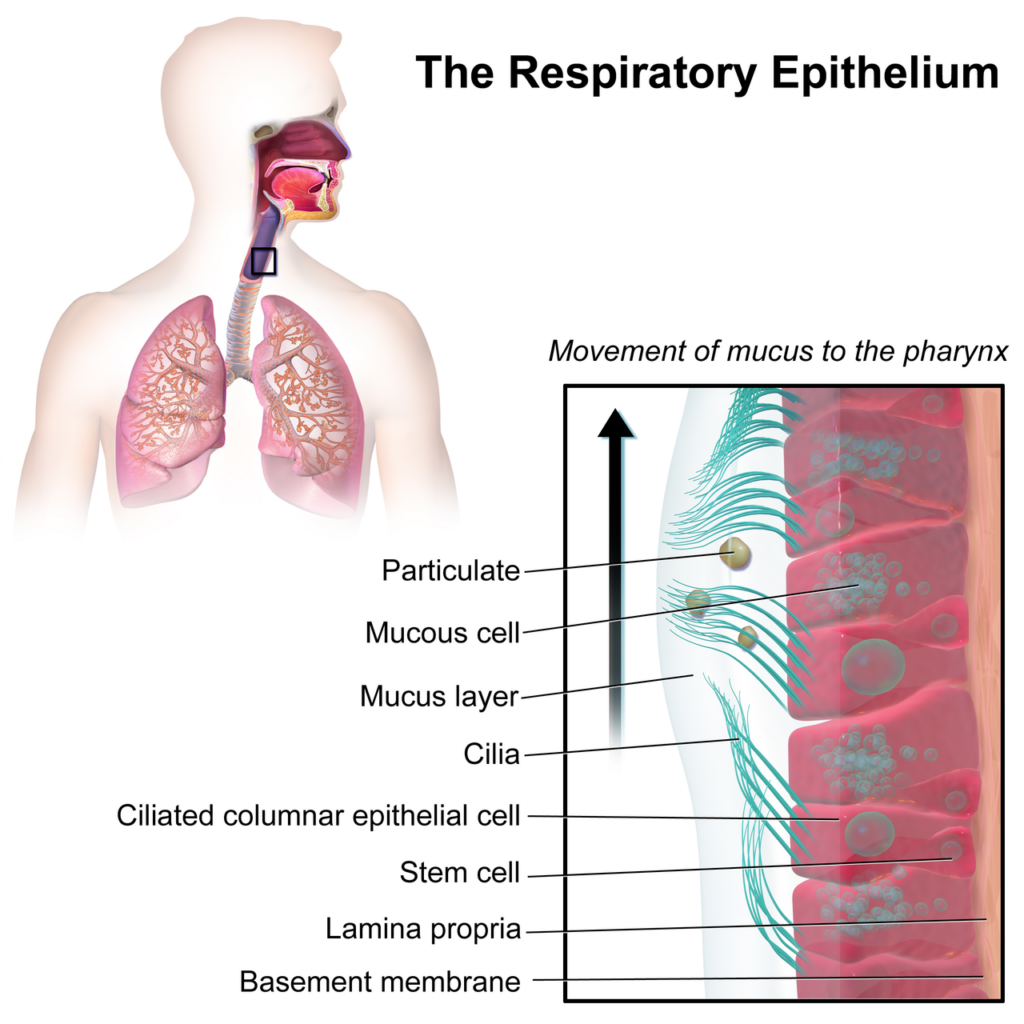
https://en.m.wikipedia.org/wiki/Cilium
精子細胞の鞭毛にも線毛運動と類似する鞭毛運動が起こります。
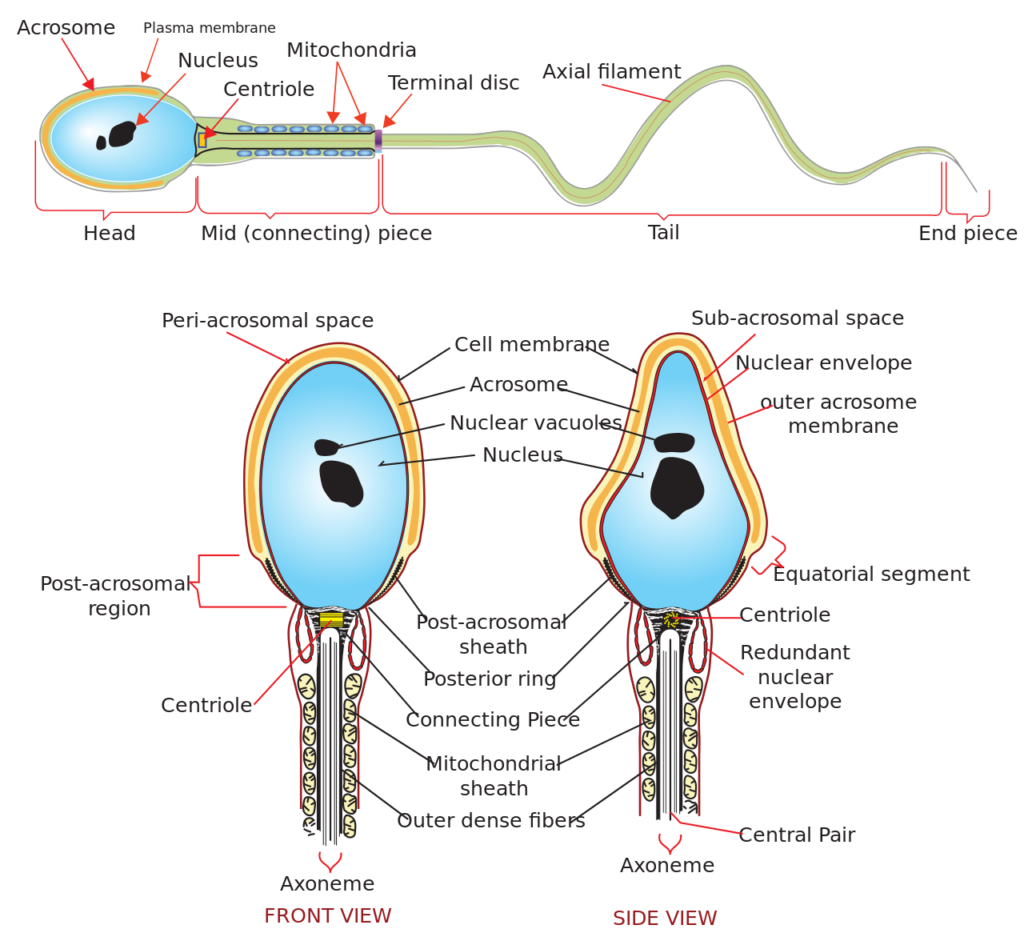
尾部に鞭毛運動の機能を有している
https://ja.m.wikipedia.org/wiki/%E7%B2%BE%E5%AD%90
生体内のこれらの部位に線毛運動機能があります。そのため、線毛運動に異常があるこの疾患(PCD)は、これらの部位に異常を起こし、それに随伴する臨床症状を起こしてきます。
臨床症状は?
線毛は気管、気管支、鼻副鼻腔を中心に存在しています。線毛運動不全があると気道に入り込んだウイルスや細菌を排除できません。
そのため、PCDでは一般に、幼少時から上気道、下気道の感染症を繰り返し起こします。
臨床症状では、肺炎、気管支炎、副鼻腔炎、中耳炎などが、慢性化して再発しやすくなります。しかしながら目立った外表奇形などがないために、幼少時期には気づかれにくく、年長児になっても診断がつかないこともしばしばみられます。
PCDの約半数が18歳以下では診断がつかなかったという報告があります。
肺・気管支
PCDは、ほぼ全例に気管支拡張症を認めます。
気管支拡張症は小児期からみられ、進行性です。区域性の無気肺(換気ができない肺の部分)が見られることが多く、PCDに特徴的です。
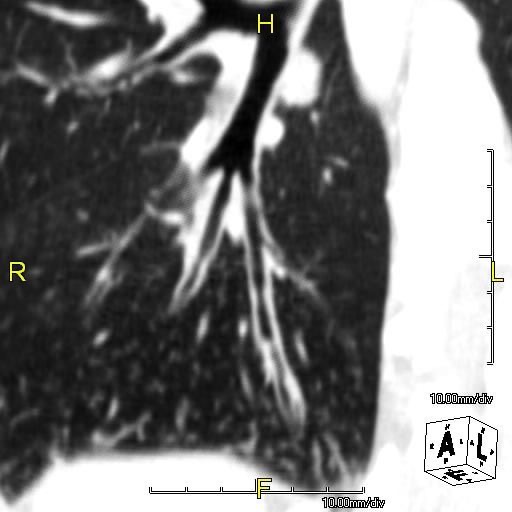
気管支拡張症を認める
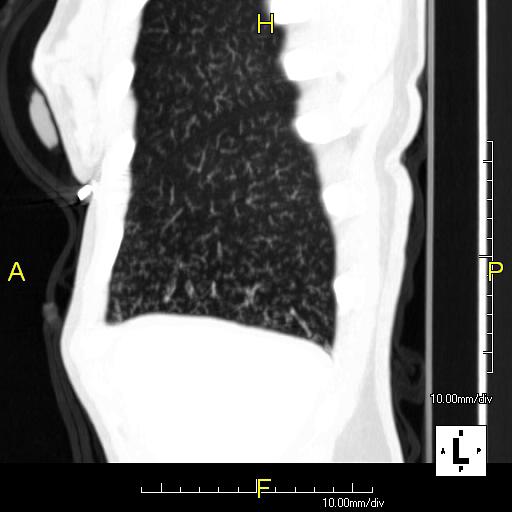
粘液栓が抹消の気管支に詰まっている
PCDの患者さんの肺は、気道上皮粘膜の線毛運動機能不全によって粘液を排出できないため、肺の細い気管支に”粘液栓”が詰まってしまい、あたかも”木の芽(tree in bud)”のよう写ります。(写真3)
副鼻腔炎
PCDでは、副鼻腔の粘膜の線毛運動機能は著しく低下します。そのため、乳幼児期から副鼻腔炎を繰り返し起こしてきます。
臨床的には、鼻茸のない慢性副鼻腔炎が特徴です。鼻腔内に粘膿性鼻漏が多量に観察され、副鼻腔手術(ESS)を行なった後も粘膿性鼻漏が改善されません。
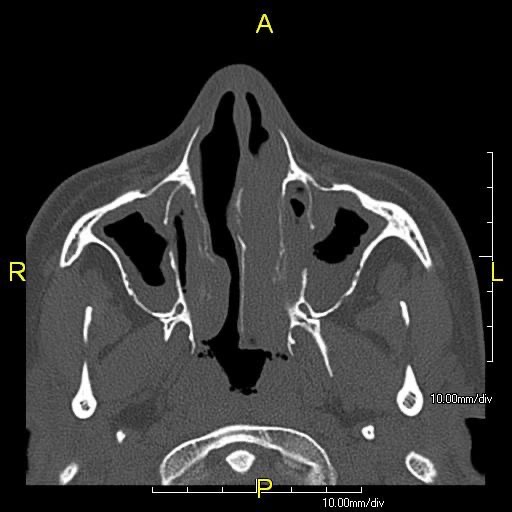
副鼻腔CTでは必ずしも高度な副鼻腔炎を認めませんが、左右の副鼻腔の空間のうち、前頭洞と蝶形骨洞の発育が未発達であることが、この疾患に特徴的であると報告されています。
中耳炎
PCDは、滲出性中耳炎を起こします。
小児では難治性の滲出性中耳炎を、成人では持続性の中耳炎を認めます。難治性滲出性中耳炎では、鼓膜換気チューブを挿入しても耳漏が停止しません。中耳粘膜の線毛運動機能の低下があるのがその理由です。この耳漏は感染による耳漏ではなく、線毛運動機能の異常によるものです。
内臓逆位
ダイニン腕の欠損があると、胎生初期に左向きの線毛運動による水流を起こす”ノード線毛”の運動障害が起こり、臓器の左右非対称配置がうまく進みません。そのため50%の確率で、左右の内臓が完全に逆転した位置にある “内臓逆位” が生じます。
一部の例では完全な内臓逆位でなく、脾臓の異常や心奇形をともなう “内臓錯位” といわれる現象も起こります。
不妊症
男性は精子の運動機能に障害がでるため、不妊症の原因になります。 (図12)
また女性でも、卵管の線毛運動機能異常によって、不妊症の原因になることが報告されています。
PCD = 副鼻腔気管支症候群?
国内でのPCDの疾患概念は、副鼻腔炎気管支症候群(sino bronchitis)という疾患と類似しているため、ほぼ同一と考えられています。
副鼻腔気管支症候群(sino bronchitis) とは、慢性副鼻腔炎と気管支拡張症を合併する疾患群です。”内臓逆位”(左右の内臓が完全に反対側に位置している)を伴うことが多いとされています。
PCDの患者さんの約50%に内臓逆位を合併することが報告されており、PCDの疾患の中で、①慢性副鼻腔炎、②気管支拡張症、③内臓逆位の3つを伴うものを”カルタゲナー症候群”(Kartagener syndrome) と呼んでいます。
逆に内臓逆位がある場合、25%はPCDであるとされています。
PCDの内臓逆位は、先に書いた、胎生期の線毛運動障害が原因と言われています。
PCDを疑うとき -診断
PCDは、さまざまな臨床症状を呈する疾患です。鼻副鼻腔炎、中耳炎、気管支肺病変、不妊症など。線毛が存在する体の部位には全て、症状が起こるからです。
50%に内臓逆位がありますので、PCDの可能性が疑われますが、反対に50%は内臓の位置は正常ですから疾患の存在そのものが疑われません。
では、どのような時にPCDを疑ったら良いのでしょうか。
まずPCDの患者さんはほとんど全例、慢性咳嗽(がいそう)があります。咳は湿性(ゼロゼロ)の咳です。したがってまず、
「幼少期から毎日のように湿性の咳があるか?」の質問にイエスと答えた患者さんに、原則として診断を行なっていきます。
PICADAR (Primary CiliAry DyskinesiA Rule) スコア
①早産か満期産か?
②新生児期に多呼吸、咳嗽、肺炎などがあったか?
③NICUに入ったか?
④内臓逆位か臓器の位置異常があるか?
⑤先天性心疾患があるか?
⑥1年を通して持続する鼻炎があるか?
⑦滲出性中耳炎、難聴、鼓膜穿孔のどれかがあるか?
②-⑦の質問にはい/いいえ で回答し、点数化する。
①は満期産/早産として2/0, ②,③,⑤ 2/0, ⑥,⑦ 1/0, ④ 4/0
合計点が6点以上を疑い例として精査する。
5点で11%, 6点で24%, 7点で44% PCDであると言われています。
PICADAR: a diagnostic predictive tool for primary ciliary dyskinesia
Laura Behan, Borislav D. Dimitrov, Claudia E. Kuehni, Claire Hogg, Mary Carroll, Hazel J. Evans, Myrofora Goutaki, Amanda Harris, Samantha Packham, Woolf T. Walker, Jane S. Lucas
European Respiratory Journal 2016 47: 1103-1112; DOI: 10.1183/13993003.01551-2015
https://erj.ersjournals.com/content/47/4/1103
PCDの診断スクリーニング検査として、①鼻腔内NO(一酸化窒素)濃度測定、②線毛の打数と打ち方を調べる高速ビデオ顕微鏡検査、③線毛運動に関わる主要タンパクの免疫染色、④電子顕微鏡による線毛横断面の微細形態の観察、⑤血液による遺伝子検査などが行われています。
とくに①鼻腔内NO(一酸化窒素)濃度測定は感度が高く、PCDでは鼻腔内NO濃度が低値になります。
画像検査として、副鼻腔CT、胸部CT、腹部CTなどで副鼻腔炎、気管支拡張症、無気肺、内臓逆位などを調べます。
④電子顕微鏡検査による線毛の微細形態の観察では、現在までに線毛の形態異常を全く認めないPCD遺伝子の存在が次々と報告されているため、形態異常がなくてもPCDを否定できなくなっています。
⑤血液による遺伝子検査の診断確率は70-75%と報告されており、これも1/4の例では診断が困難になっています。
鼻腔内NO(一酸化窒素)濃度測定は、たとえ低値でなくてもPCDは否定できず、さらなる解析を必要とするとされています。
PCDを疑うとき -症状
では実際、どんな症状のときに、PCDを疑ったら良いのでしょうか。
PCDの症状をまとめると、「生後まもなく、そして幼少期から現在にいたるまで、慢性湿性咳嗽があって、副鼻腔炎、中耳炎、気管支拡張症、内臓逆位がある」患者さん、と言えそうです。
これを医学用語を使わずにできるだけ簡単に言うと、表現が100%正確ではありませんが、以下のようになります。
「小さい頃からゼロゼロの咳がずっと続いていて、喘息みたいだと言われています。(または ” 喘息として治療されています。” )
そう言えばこの子は生まれた時、呼吸の状態が悪いとか何とかで、しばらくNICUに入っていました。
この子は風邪を引きやすくて、風邪を引くとすごく長引いて、いつまでも咳が続いたりゼロゼロした痰が絡んで苦しそうにしています。
ずっと蓄膿(ちくのう)症があって、黄色いネバネバした鼻水がたくさん出て、喉に流れてきます。耳鼻科で薬をもらっていますが、粘っこい鼻水が治りません。中耳炎がなかなか治らずに、何度も鼓膜切開をしています。鼓膜チューブを入れてもらったけど、耳垂れが止まりません。」
「内臓の位置が反対にあると言われました。」(50%の患者さん)
治療は?
PCDの根本的な治療方法はまだ見つかっていません。
粘膜の線毛運動機能の障害なので、基本的に耳鼻咽喉科での治療が奏功しません。
したがって、改善がない粘膿性鼻漏(黄色い粘っこい鼻水)、止まらない耳漏、ゼロゼロの湿性咳が続いている、などの辛い症状が持続します。
現在までの報告では、①PCDに合併した慢性副鼻腔炎に対しては、ESS後も粘膿性鼻漏は停止せず、②滲出性中耳炎に対して行われる鼓膜チューブ留置術後も耳漏が継続してみられることが報告されています。
③気管支拡張症に対しては、クラリス錠、アジスロマイシン錠などを内服すると、肺病変や呼吸機能の改善がみられた例が報告されており、マクロライド治療が効果を示す成績が示されています。
また、本人の喫煙や受動喫煙が非常に危険であることが言われているため、患者さん本人への知識の共有がとても大切になっています。
また、クラリス錠の内服は、慢性副鼻腔炎に対しても一定の効果を上げることがわかってきており、治療として実施されることが期待されます。
高度の副鼻腔炎に対してはESS(内視鏡下副鼻腔手術)で膿性鼻漏の停止はできませんが、副鼻腔炎そのものを改善することで、鼻閉の改善などから後鼻漏や膿性鼻漏を少しでも減少させる効果はあると考えられており、二次的な効果を含めると全く適応にならないわけではありません。その点は主治医とよく相談すべきと思います。
肺の気管支拡張症に対しては、気道感染症による呼吸状態の悪化を防ぐため、感染予防はもとより、気道感染が疑われたときは早期の抗菌薬投与が勧められています。各種ワクチン接種によるウイルス感染予防も非常に有効です。
PCDの診断が確定したら、耳鼻咽喉科医だけでなく、呼吸器科医、内科医、場合によって、産婦人科医などとも連携して、複数科による総合的な治療を行っていくのが最良の方法です。
考えること
PCDは、2万人に1人の希少疾患です。
風邪やふつうの中耳炎のように、どこにでもある、ありふれた病気ではありません。
そのために、治療を受ける方も、治療をする方も、ともすれば診断を見落としがちになる病気です。実際にPCDの診断率は決して高くありません。内臓逆位を伴わない例では、小児期に診断されにくく、成人になってようやく診断が確定する例も珍しくありません。
では具体的に私たちは、一体何をすれば良いのでしょう。
病気を疑ってください
それは、疾患を疑うことです。
誤解を恐れずに言えば、1人の医師が診断する疾患には限界があります。理由は、全診療科に堪能な医師はほとんどいないからです。
とくにこの疾患のように、非常に数少ない疾患であればあるほど、1人の医師の力では限界もあると思います。
それは、その医師の診断力や診断技術だけを言っているのではありません。症状が全身に及んでいる疾患のため、1人の医師だけではその疾患の断片的なものしか見ていないことがあるからです。
小児科医は小児科医の立場から、呼吸器科医は呼吸器科医の立場から、そして耳鼻咽喉科医は耳鼻咽喉科医の立場から、患者さんを診ています。その3人がうまく連携が取れた時、診断力は何倍にもなって、患者さんの真の病態が見えてきます。
でも、ふつうはそうはいかないことの方がずっと多いと思います。ですから、医師の診断は、常に100%ではないことを思っていてください。
患者さんも一緒になって考えましょう。
医師のせいばかりではありません。
子どもさんのあらゆる症状を細かく観察して医師に伝えるのも、患者さんのご家族の大切な役目です。
医師は1日中その子を観察しているわけではありません。ご家族からの何気ない一言によって医師が気づくことも多いからです。
もし、あなたのお子さんにこのような症状が疑われるとき、かかりつけの耳鼻咽喉科医だけでなく、小児科医や呼吸器科医、内科医の先生方に思い切って尋ねてみましょう。
この子はどうして治らないのですか?
何か、別の病気はないのでしょうか?
と。

(イメージです)